Контроль качества лабораторных исследований
Для обеспечения качества исследований лаборатории осуществляют:
Внутрилабораторный контроль (ВЛКК): оперативный контроль качества результатов до их передачи для клинического использования.
Внешняя оценка качества (ВОК): ретроспективная оценка качества результатов после их клинического использования, оценка эффективности внутрилабораторного контроля.
Целью модуля контроля качества МИС КСАМУ является оказание помощи КДЛ в обеспечении выполняемых исследований путём предоставления им:
- Информации о правильности получаемых результатов;
- Рекомендаций по устранению используемых методик и внутрилабораторной системы обеспечения качества.
ВЛКК в КДЛ – это целый комплекс мероприятий, направленных на обеспечение качества и недопущение погрешностей измерений исследований.
ВЛКК включает следующие этапы:
- Преаналитический этап (внелабораторная и лабораторная части этапа)
- Аналитический этап
- Постаналитический этап
Наличие системы ВЛКК является одним из критериев аккредитации лаборатории и учитывается при лицензировании медицинской деятельности.
ВЛКК обязателен в отношении всех видов количественных исследований, выполняемых в КДЛ, для которых разработаны контрольные материалы.
ВЛКК должен проводиться постоянно сотрудниками каждой лаборатории при измерении каждого аналита в каждой аналитической серии.
Контрольные материалы исследуются также как и образцы пациентов.
Проверку наличия системы ВЛКК в КДЛ осуществляют территориальные органы Здравоохранения.
Организация и обеспечение ВЛКК является обязанностью заведующего лабораторией или сотрудника, ответственного за обеспечение качества.
Порядок проведения ВЛКК
Стадия 1. Оценка повторяемости (сходимости) результатов измерений.
Используются контрольные материалы (КМ) или пробы пациентов со значением определяемого показателя в нормальном диапазоне.
Стадия 2. Оценка прецизионности (воспроизводимости) и относительного смещения (правильности) по результатам установочной серии измерений, построение контрольных карт.
Используются контрольный материал промышленного производства в двух диапазонах определяемого показателя.
Стадия 3. Проведение оперативного ВЛКК в каждой аналитической серии.
Используются контрольный материал промышленного производства в двух диапазонах определяемого показателя.
Контрольные материалы
Контрольный материал (КМ) – натуральный или искусственный однородный материал, содержащий те же компоненты, что и пробы пациентов.
- Самостоятельно изготовленные (слитые сыворотки, Приказ № 45).
- Промышленные:
- Аттестованные (контроль правильности и воспроизводимости, 2 этап)
Имеют известное значение измеряемых характеристик КМ, установленное при его аттестации и приводимое в паспорте и других документах на КМ).
- Неаттестованные (контроль воспроизводимости, 1 этап)
Значение аналитов не известно.
Внутрилабораторный контроль качества с использованием контрольных материалов должен выполняться в течение достаточно длительного времени с использованием одного и того же контрольного материала - на протяжении не менее 200 аналитических серий (для гематологических анализаторов – не менее 40 серий).
Контроль качества в интерфейсе МИС КСАМУ
Все документы, необходимые для документального сопровождения внутрилабораторного контроля качества доступны в интерфейсе МИС КСАМУ по пути Документы > Лаборатория > Контроль качества.
Стадия 1. Оценка повторяемости (сходимости) результатов измерений.
Оформление оценки сходимости результатов измерений доступно из пункта меню Документы > Лаборатория > Контроль качества > Оценка сходимости результатов измерения (Рис. 1 п. 1).
В этом документе основными элементами являются:
- Параметр лабораторного исследования.
- Оборудование ЛПУ, на котором произведено исследование.
- Методика измерений параметра лабораторного исследования (Рисунок 3).
- Допустимые значения – ссылка на справочник «Предельно допустимые значения». Справочник заполнен из приложения А ГОСТ Р 53133.2-2008
- Контрольный материал, используемый для оценки сходимости. В примере на Рис. 2 указан признак «Проба пациента», подразумевающий самостоятельно изготовленный контрольный материал. Контрольный материал – ссылка на справочник «Номенклатура» (Рис 5). Если Вы используете аттестованный контрольный материал, выберите его из открывшегося справочника, укажите номер партии (Рис. 6), укажите аттестованные значения.
- Блок используемого реактива (Реагент). Выберите используемые реактивы из справочника «Номенклатура», рис. 5. После этого укажите в соответствующее поле номер партии реагента, рис. 6.
- Коэффициент вариации – визуализация контрольных значений, где: CVw – вычисленный на основе 10 контрольных измерений (Рис. 2 п. 8) коэффициент вариации. MAX CV10/2 – значение CV10, полученное из выбранного элемента справочника «Предельно допускаемые значения» (указывается в рис. 2, п.4), делённое на 2.
- Результаты 10 измерений, требуемые для вычисления CVw.
Последовательность выполнения стадии 1:
- Указать допустимые значения (Рис. 2, пункт 4).
- Провести 10 измерений в одном и том же контрольном материале (Рис. 2 п.5) в одной аналитической серии.
- Результаты измерений внести в регистрационную форму (Рис. 2, п.8)
- Проверить выполнение правила.
Правило 1 стадии:
Если вычисленный на основе 10 измерений коэффициент вариации CVw не превышает половину предельно допустимого значение смещения MAX CV10/2, перейдите к стадии 2. В интерфейсе документа, в случае положительного прохождения правила 1 стадии, появится надпись «Повторяемость соответствует установленным нормам» (Рис. 2 п.9).
Если CVw больше, чем MAX CV10/2 следует выявить источник недопустимо больших случайных погрешностей и повторить 1 стадию с начала. В интерфейсе документа (рис. 2 п.9), в случае негативного результата проверки правила 1 стадии, появится надпись (Рис. 7) «CVw превышает 0,5 CV10, необходимо выявить источники недопустимо больших случайных погрешностей и провести работу по их устранению. Затем повторить оценку сходимости результатов измерения».
Стадия 2. Оценка прецизионности (воспроизводимости) и относительного смещения (правильности) по результатам установочной серии измерений, построение контрольных карт.
Оформление оценки воспроизводимости и правильности результатов измерений доступно из пункта меню Документы > Лаборатория > Контроль качества > Оценка воспроизводимости и правильности результатов измерений (Рис. 1 п. 2).
В документе (Рис. 8) основными элементами являются:
Вкладка «Контрольные материалы»:
- Оценка сходимости – документ, заполняемый на стадии 1. Из документа заполняются поля: Параметр. Методика. Оборудование.
- Дата измерения – автоматически заполняемые на основании результатов измерений поля. Подставляется минимальная и максимальная даты соответственно.
- Блок используемого реактива (Реагент). Выберите используемые реактивы из справочника «Номенклатура», рис. 5. После этого укажите в соответствующее поле номер партии реагента, рис. 6.
- Используемый контрольный материал № 1. Укажите аттестованное значение КМ, а также минимум и максимум отклонения от аттестованного значения (если есть). Выберите используемый реактив из справочника «Номенклатура», рис. 5. (если есть), а также номер партии реактива рис. 6.
- Используемый контрольный материал 2. Укажите аттестованное значение КМ, а также минимум и максимум отклонения от аттестованного значения (если есть). Выберите используемый реактив из справочника «Номенклатура», рис. 5. (если есть), а также номер партии реактива рис. 6.
Вкладка «Результаты измерений»:
1) Результаты измерения контрольных материалов в 20 аналитических сериях одновременно в двух контрольных материалах (рис. 9 п.1).
Порядок заполнения:
1.1) Производится постановка 10 аналитических серий.
На основании 10 аналитических серий происходит предварительная оценка погрешностей в установочной серии. Вычисляются (в блоке «Коэффициенты и допуски», рис. 9 п.2):
- X – среднеарифметическое значение;
- – среднеквадратичное отклонение в 10 аналитических сериях;
- CV10 – прецизионность в 10 аналитических сериях;
- B10 – относительное смещение (правильность) 10 аналитических сериях.
Полученные значения CV10 и B10 сравниваются с предельно допустимыми значениями (рис. 4). Если полученные значения превышают допустимые, следует выявить погрешности и провести работу по их устранению.
1.2) Если полученные значения не превышают установленных норм, выполняются следующие 10 аналитических серий. Вычисляются:
- X – среднеарифметическое значение (перерасчёт);
- S – среднеквадратичное отклонение в 20 аналитических сериях (перерасчёт);
- CV20 – прецизионность в 20 аналитических сериях;
- B20 – относительное смещение (правильность) 10 аналитических сериях.
Правила 2 стадии:
- Если полученное значение CV20 превышает допустимое, следует выявить источники погрешности и провести работы по их устранению. Затем провести повторные измерения.
- Если значения коэффициента вариации CV20 не превышает установленных норм, следует сравнить рассчитанное значение B20 с предельно допустимым значением B20 (рис. 4). Если значение B20 превышает допустимое, следует установить причину отклонения и устранить её. Затем провести повторные измерения. Пример превышения допустимых значений (выделено красным) отображен на рис. 10.
- Если значение B20 не превышает допустимое, делают вывод о возможности использования рассматриваемой методики для целей лабораторной диагностики. На основании 20 измерений в контрольных пробах происходит построение контрольных карт.
Вкладка «Контрольная карта».
Выполненные измерения двадцати лабораторных показателей в контрольных материалах называют установочными сериями измерений, по результатам которых рассчитывают среднеарифметическое значение X, среднеквадратическое отклонение S и контрольные пределы для каждого контрольного материала. Устанавливаются контрольные пределы (X ± 1S), (X ± 2S), (X ± 3S). На основании вычисленных значений происходит построение контрольных карт.
Контрольная карта, построенная на установочной серии измерений, представляет собой график, на оси абсцисс которого откладывается номер аналитической серии (рис. 9, п.1 столбец номер) (или дата ее выполнения), а на оси ординат – значения определяемого показателя (рис. 9, п.1 столбец значение) в контрольном материале (рисунок 11).
4. Если в ряду результатов оказалось значение, выходящее за пределы (X ± 3S), то его не учитывают, выполняют ещё одну аналитическую серию, после чего снова подсчитывается (перерасчёт происходит автоматически): среднеарифметическое значение X, среднеквадратическое отклонение S.
Стадия 3. Проведение оперативного ВЛКК в каждой аналитической серии.
Оформление протокола оперативного внутрилабораторного контроля качества доступно из пункта меню Документы > Лаборатория > Контроль качества > Оперативный внутрилабораторный контроль качества (Рис. 1 п. 3).
Цель данного этапа: оценка приемлемости результатов исследования проб пациентов и подтверждение стабильности аналитической системы по результатам исследования контрольных материалов в каждой аналитической серии.
Для получения исходных данных, на основе которых будет строиться контрольная карта, указывают документ, оформленный на 2 стадии «Оценка воспроизводимости и правильности» (Рис 12, п.1). Данные из «Протокол оценки…» используются для вычисления среднеарифметической величины Х, среднего квадратичного отклонения S и вычисления контрольных пределов Х±1S, Х±2S и Х±3S отображение данных величин визуализируется в блоке «Значения Контрольной карты», рисунок 12, пункт 4.
Последовательность выполнения оперативного контроля:
- В каждой аналитической серии проводится однократное (как минимум) измерение показателя в каждом контрольном материале. Число образцов пациентов в аналитической серии не ограничивается.
- Заносятся результаты измерений контрольного материала в аналитической серии в табличную часть «Результаты измерений» (рис. 12, п 2 и 3, столбец «Значение»).
- При отклонении результатов контрольных измерений за контрольные пределы оценить приемлемость результатов проб пациентов в данной аналитической серии с помощью контрольных правил.
Правила 3 стадии (проверки происходят автоматически):
Правило 12S. Если один из результатов анализа контрольных материалов выходит за пределы (X ± 2S). Правило является предупредительным, его выявление не должно приводить к отбраковке результатов аналитической серии и повторному исследованию проб. Следует последовательно проверить правила 13S, 22S, R4S, 41S и 10X. Аналитическая серия признаётся неудовлетворительной выполнении одного из них:
Правило 13S. Одно из контрольных измерений выходит за пределы (X ± 3S). Данный признак свидетельствует о наличии грубой погрешности
Правило 22S. Два последних измерения в рассматриваемой аналитической серии превышают (X + 2S) или лежат ниже (X - 2S). Признак свидетельствует о систематической ошибке методики.
Правило R4S. Два контрольных измерения в рассматриваемой аналитической серии расположены по разные стороны от коридора (X ± 2S). Признак свидетельствует о появлении случайной ошибки.
Правило 41S. Четыре последних контрольных измерения превышают (X + 1S) или лежат ниже (X - 1S). Признак свидетельствует о систематической ошибке методики.
Правило 10X.Десять последних контрольных измерений располагаются по одну сторону от линии, соответствующей X. Признак свидетельствует о систематической ошибке методики.
Последовательность действий в случае выявления признака 12S:
- Если в дополнение к 12S выявлен хотя бы один из 13S, 22S, R4S, 41S и 10X, все результаты, полученные в данной аналитической серии, следует считать неприемлемыми. (Рисунок 15)
- Контрольные признаки 22S, 41S и 10X следует проверять на одной контрольной карте и/или на обеих контрольных картах.
- В случае неприемлемости результатов, проведение анализа следует приостановить, выявить и устранить причины возникновения повышенных погрешностей. Все пробы, проанализированные в этой серии (и пациентов, и контрольные), исследовать повторно.
- Результаты измерения контрольных материалов в серии, признанной неприемлемой, не должны использоваться при оценке по контрольным правилам повторной и последующей серий.
- В случае, если ни один из признаков 13S, 22S, R4S, 41S и 10X, не обнаруживается ни на одной контрольной карте, проведение исследований следует продолжить.
- Решение о приемлемости результатов измерения аналита в биологическом материале пациента принимается сотрудником, отвечающим за качество исследований. Если результаты аналитической серии признаются неприемлемыми, делается соответствующая запись в журнале «Регистрация отбракованных результатов внутрилабораторного контроля качества» (рисунок 16).
Для установления надежных контрольных пределов после проведения не менее 50 аналитических серий (включая установочную) рекомендуется пересчитать значения X и S (рис. 12 п.5). Контрольные карты при этом перестраиваются.
На форме оперативного КК есть настройка "количество точек". Указанное значение определяет какое количество точек отображать на графике по горизонтали. По умолчанию заполняется значение "30". Так же имеются кнопки изменения масштаба на графике (Рисунок 16)
Нарушение правил аналитической серии.
Правило 10X.
В контрольной карте оперативного контроля при наведении на выбракованную точку подсвечиваются точки, на основании которых прошла выбраковка. (Рисунок 17)
Также в таблице со значениями (на вкладке результаты измерений), при нажатии на выбракованную точку подсвечиваются точки, на основании которых прошла выбраковка. (Рисунок 18)
Регистрация отбракованных результатов
В случае выявления брака (Рисунок 19), отбракованная серия обязана регистрироваться.
Регистрация отбракованных результатов доступно из пункта меню Документы > Лаборатория > Контроль качества > Регистрация отбракованных результатов (Рис. 1 п. 4).
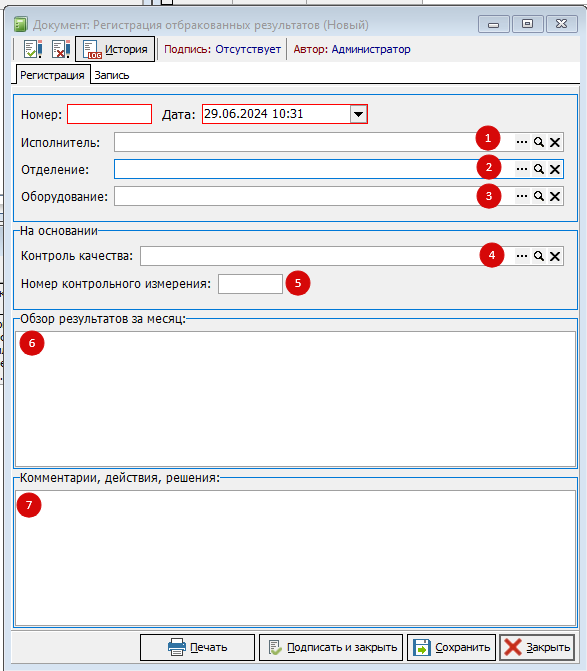
При регистрации отбракованной аналитической серии (рисунок 20), указывается:
- Исполнитель аналитической серии
- Отделение исполнителя
- Оборудование, на котором произведено измерение
- Документ – основание отбраковки (заполняется на 3 этапе)
- Номер контрольного измерения
- Обзор результатов за месяц. Заполняется заведующей лаборатории.
- Комментарии, действия, принятые решения для устранения ошибок. Заполняется заведующей лаборатории.
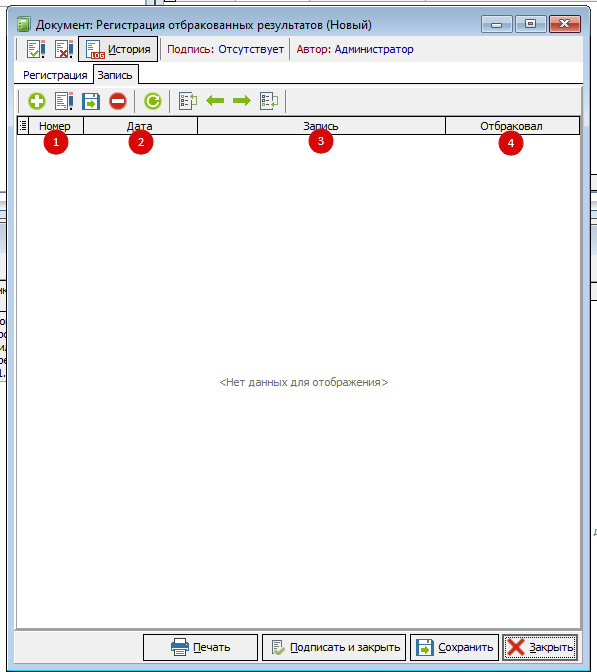
- Номер – номер контрольного измерения.
- Дата – дата отбраковки.
- Запись – перечисление произведённых действий при отбраковке (проверка калибровки, инструментов, дозирования, повторное измерение результатов отбракованной аналитической серии)
- Сотрудник, проводивший отбраковку.
Нормативные документы
Приказ МЗ РФ №220 от 26 мая 2003 г.
ОСТ «Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов».
Изложены средства, способы и порядок проведения ВЛКК на аналитическом этапе лабораторного исследования.
Приказ МЗ РФ №45 от 7 февраля 2000 г.
«Правила внутрилабораторного контроля качества количественных лабораторных исследований».
Национальный стандарт РФ ГОСТ Р 53133-2008
ГОСТ Р 53133.1-2008 - Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 1. Пределы допускаемых погрешностей результатов измерения аналитов в клинико-диагностических лабораториях.
ГОСТ Р 53133.2-2008 - Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 2. Правила проведения внутрилабораторного контроля качества количественных методов клинических лабораторных исследований с использованием контрольных материалов
ГОСТ Р 53133.3-2008 - Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 3. Описание материалов для контроля качества клинических лабораторных исследований
ГОСТ Р 53133.4-2008 - Технологии лабораторные клинические. Контроль качества клинических лабораторных исследований. Часть 4. Правила проведения клинического аудита эффективности лабораторного обеспечения деятельности медицинских организаций


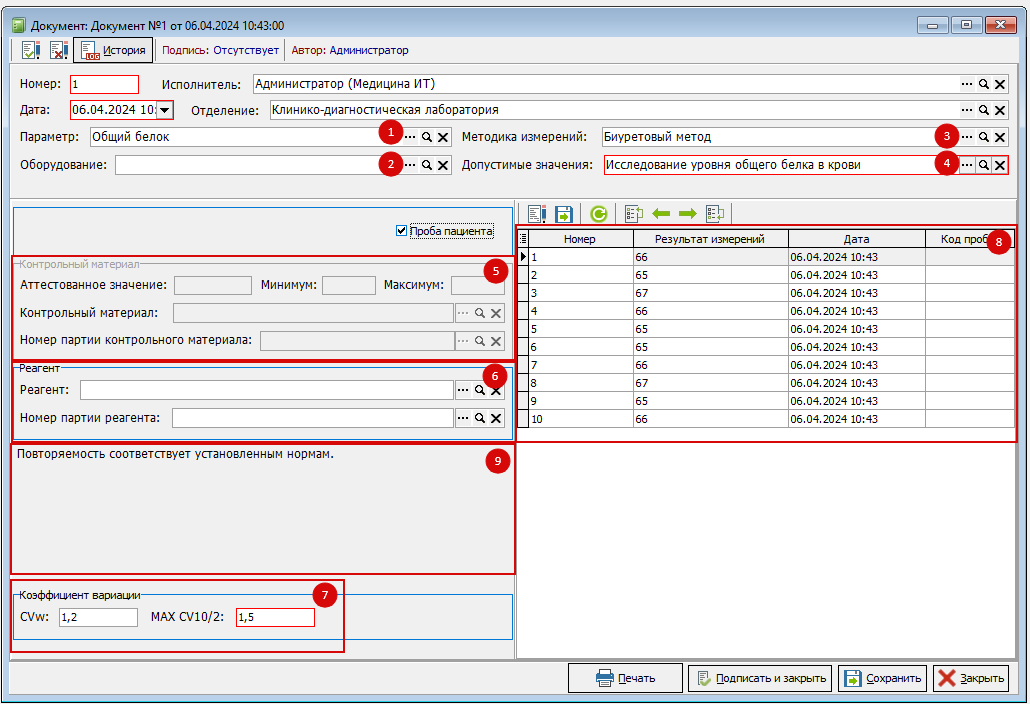
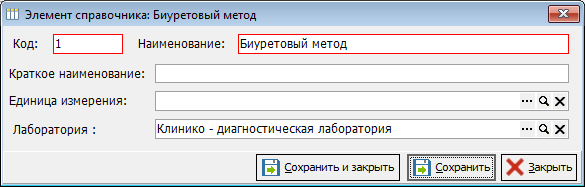
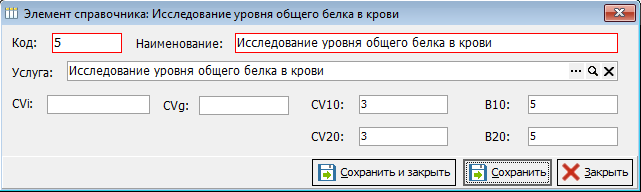
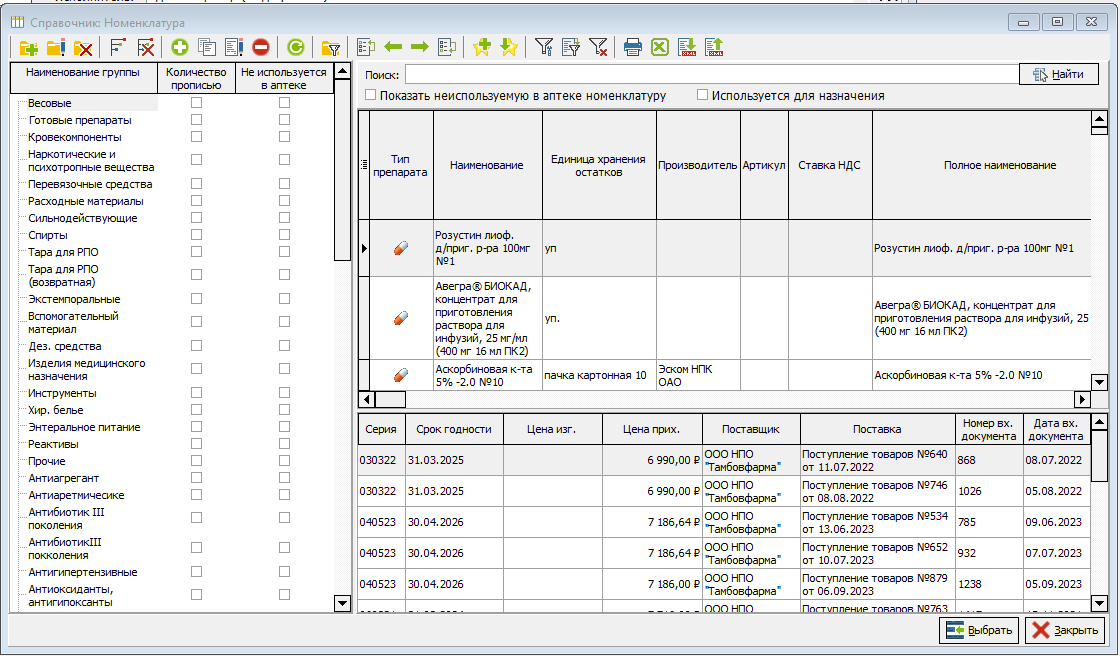
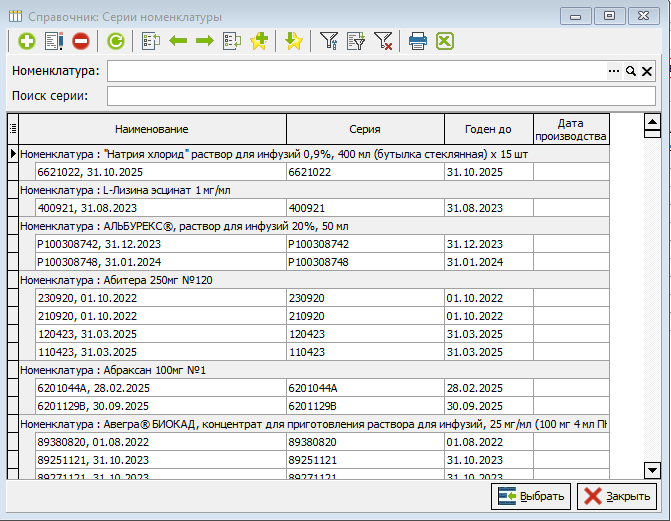

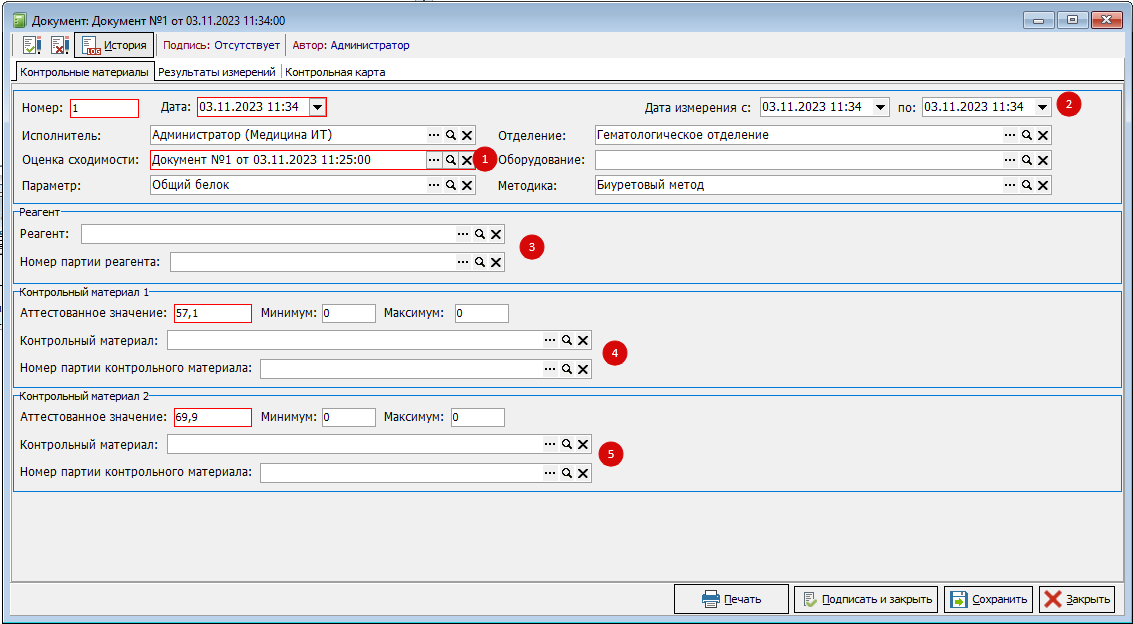
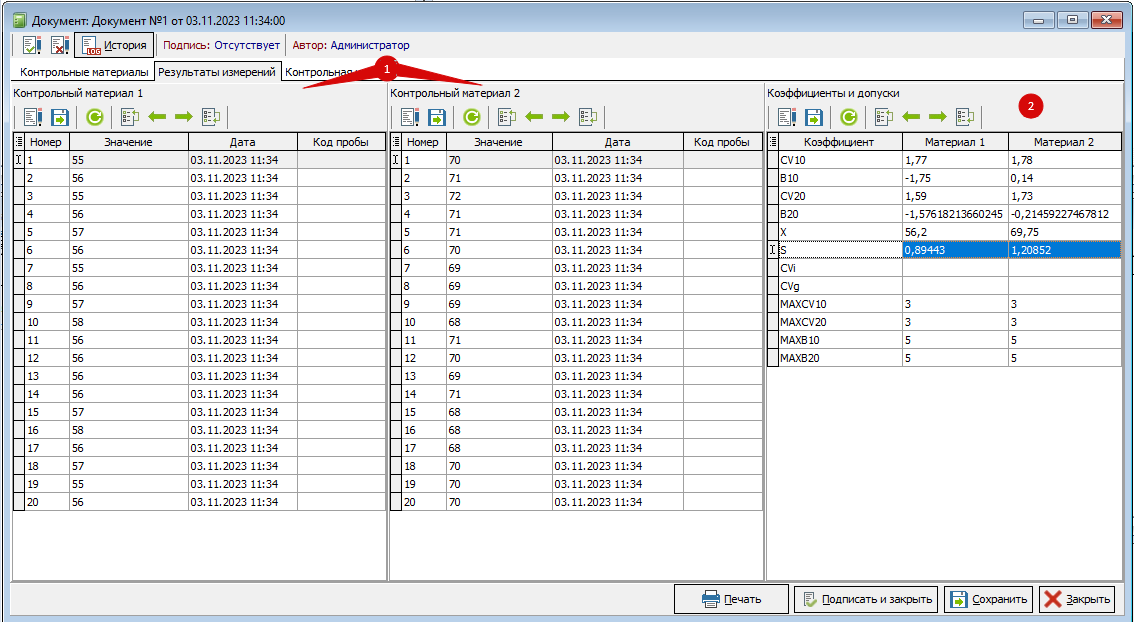
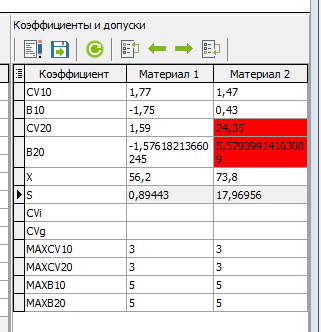
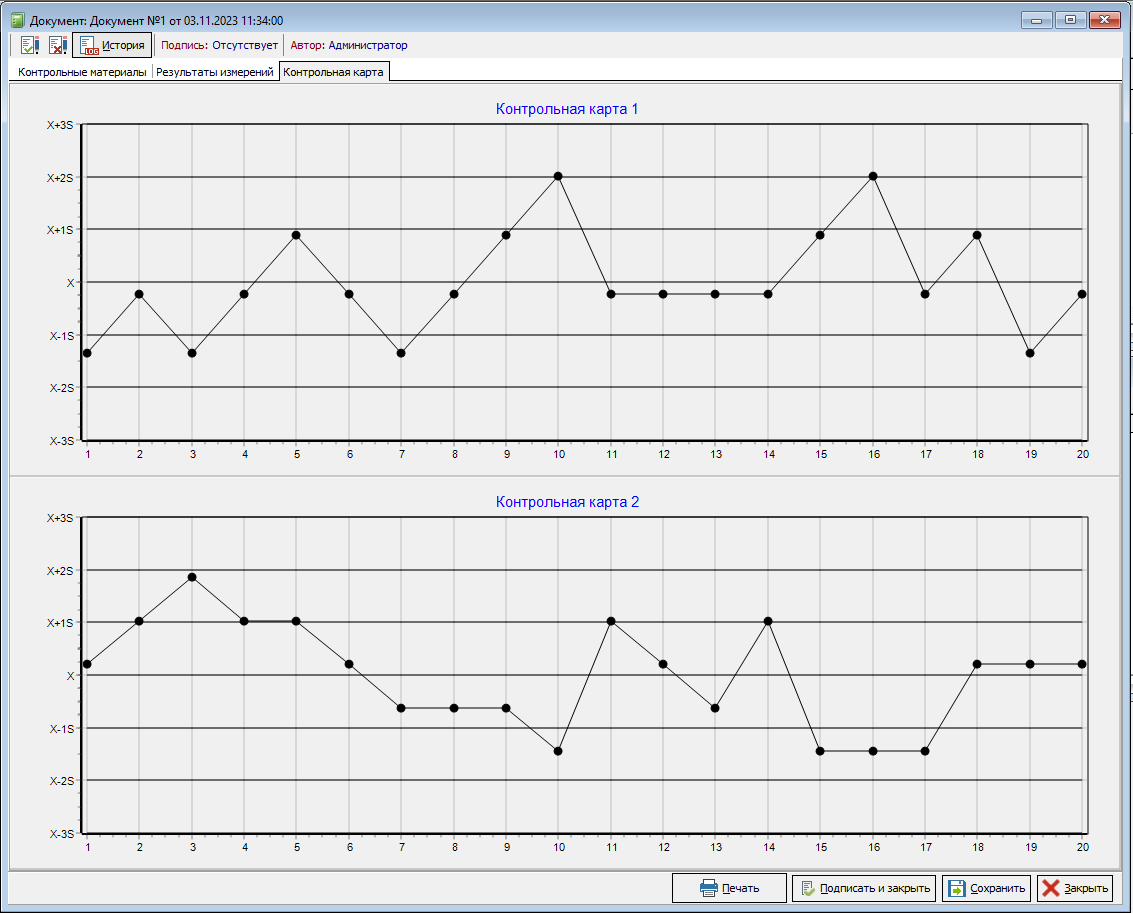
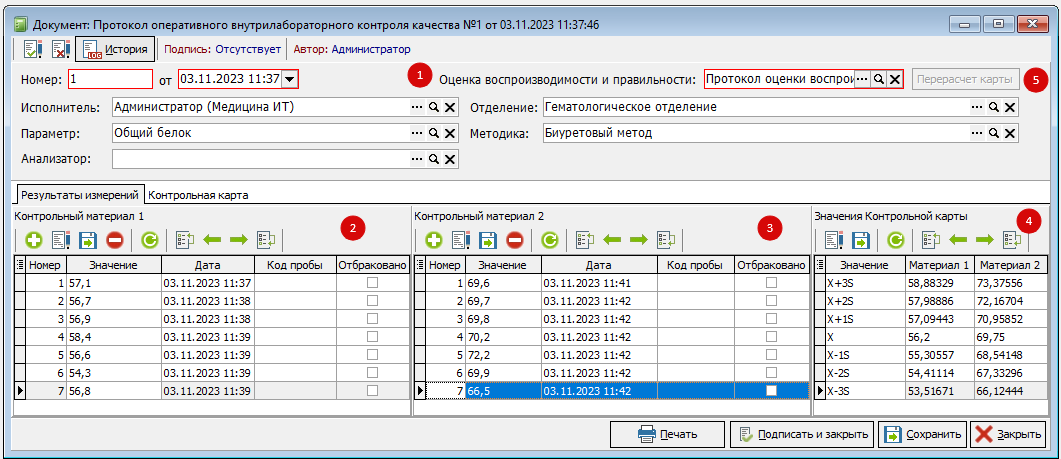
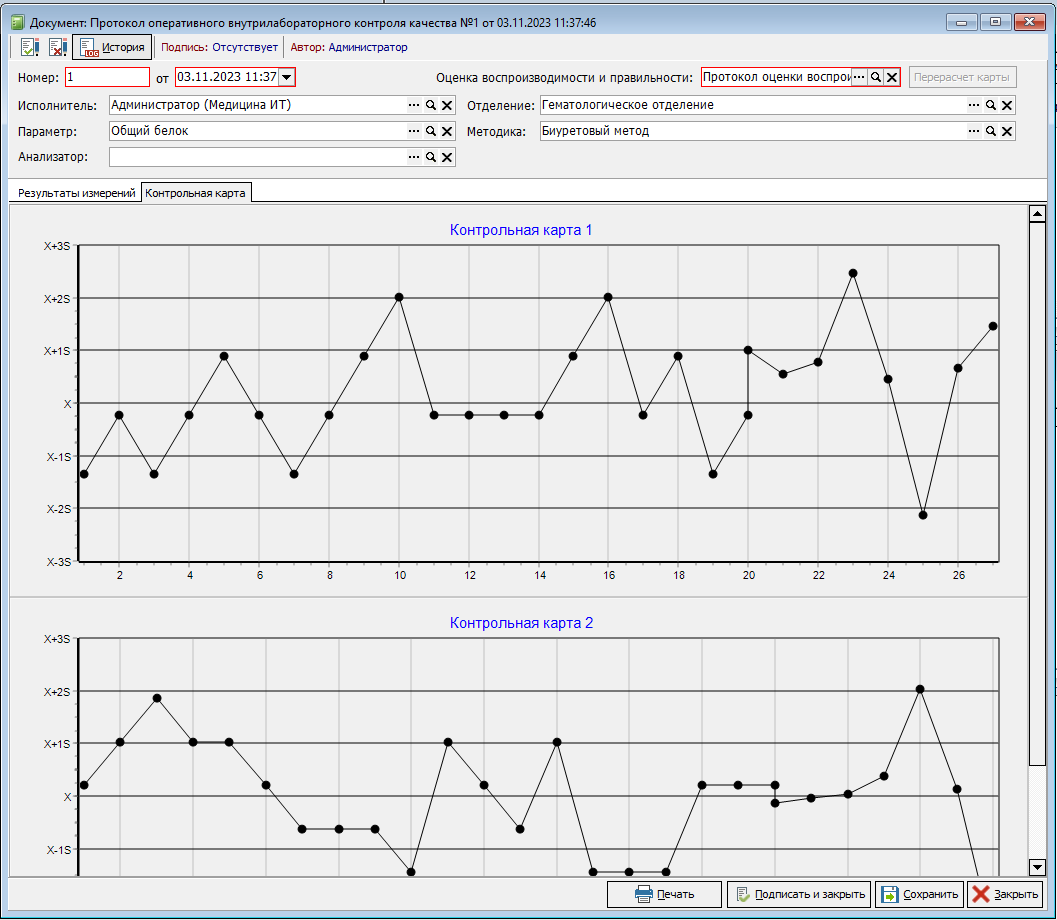
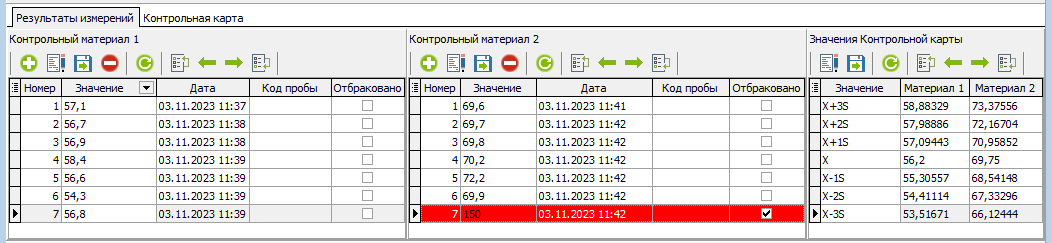
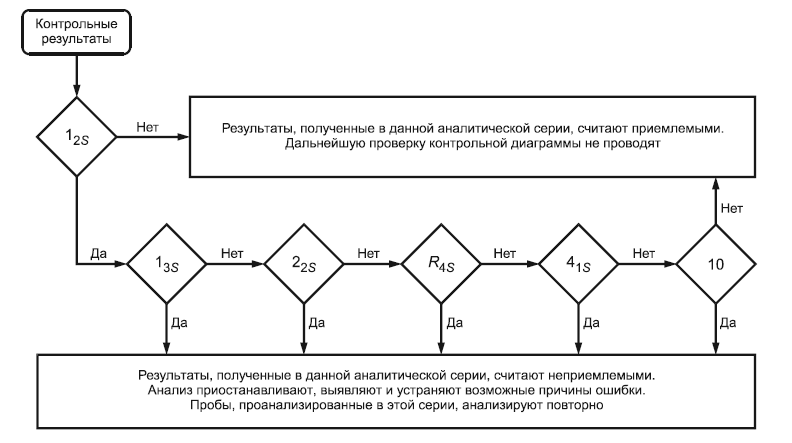
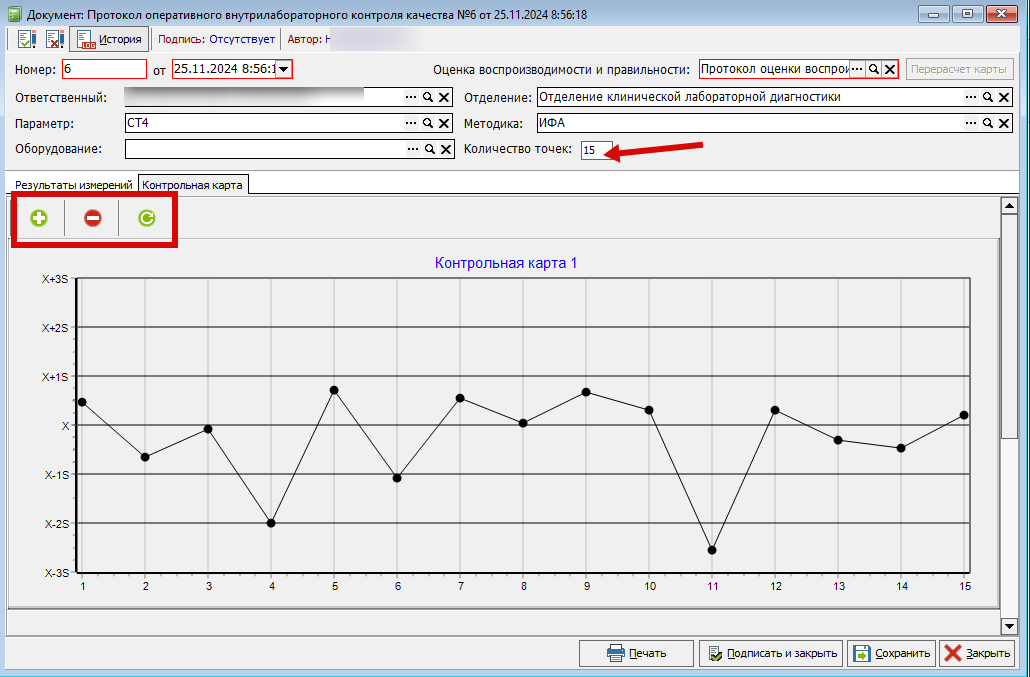
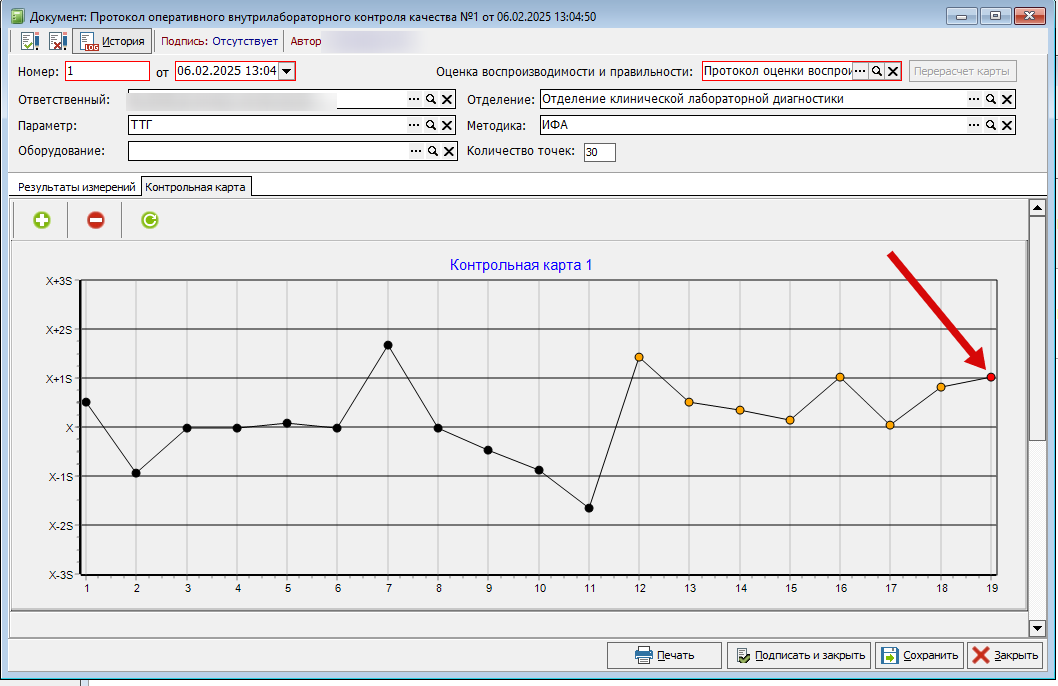 Рисунок 17
Рисунок 17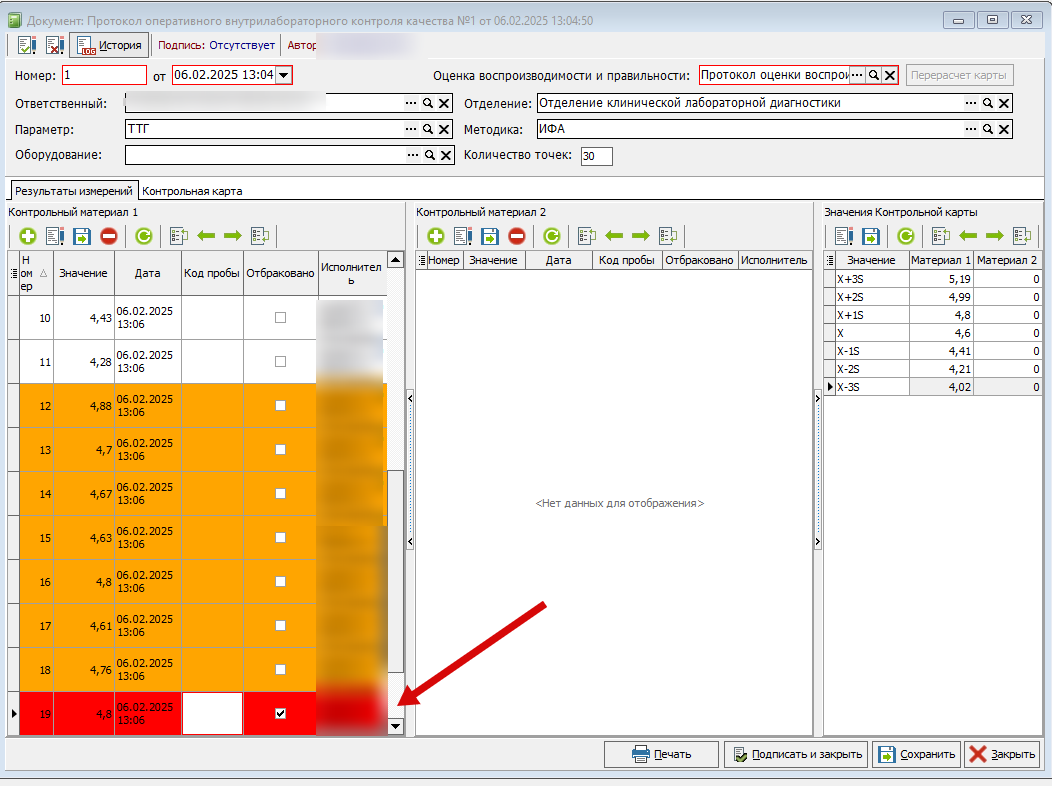
No Comments